重庆医科大学/香港中文大学团队MTB:3D打印技术助力骨骼肌器官芯片
时间:2025-08-28 12:11:33 热度:37.1℃ 作者:网络
器官芯片(OoC)是一种在微流控芯片上构建的微型人体器官模型,可模拟器官级生理与病理反应。2025年7月7日,美国食品药品监督管理局(FDA)召开专题研讨会,聚焦“减少动物实验”。会议释放明确信号:在提交新药或生物制品申请时,可优先采纳OoC等非动物实验数据,以支持安全性与有效性评价。这一动向被视为OoC技术在药物研发领域战略地位的显著跃升,或将深刻影响未来的监管框架与产业实践。
3D打印技术凭借“逐层堆积、一体成型”的优势,为复杂微生理系统的快速构建提供了关键工具。2025年8月26日,重庆医科大学黄伟、包微、雷一霆团队联合香港中文大学李中、周良彬团队在Materials Today Bio上发表综述文章“The role of 3D printing in skeletal muscle-on-a-chip models: Current applications and future potential”,系统回顾了3D打印在骨骼肌器官芯片(SMoC)构建中的作用、现有应用及未来挑战。

一、为什么骨骼肌需要“芯片化”
1. 结构复杂:肌外膜-肌束膜-肌内膜多级结缔组织包裹;肌纤维内肌原纤维与肌节排列高度有序;毛细血管、神经元、卫星细胞与免疫细胞共同组成微环境。
2. 功能多样:机械收缩、代谢产热、内分泌调控、力学感知。
3. 疾病谱广:遗传性(Duchenne型肌营养不良)、神经源性(肌萎缩侧索硬化症)、自身免疫性(重症肌无力)、炎症性(多发性肌炎)、增龄性(肌少症)等。
传统二维培养缺乏三维排列与力学刺激;动物模型存在种属差异及伦理限制,因此SMoC应运而生。
二、3D打印如何“打印”一块肌肉
1. 芯片支架——先定“房子”
• 工业级打印:熔融沉积建模(FDM)低成本快速打样;光刻(SLA)或数字光处理(DLP)提供适合微通道、锚定柱、电极插槽的精细结构。
• 模具复刻:先用刚性光敏树脂打印阳模,再用聚二甲基硅氧烷(PDMS)倒模,兼顾柔性与生物惰性,可批量复制。
• 动态接口:在打印阶段预埋电极、光纤或应变传感器,实现后续电刺激与力学监测一体化。
2. 生物墨水——再配“混凝土”
• 基体材料:甲基丙烯酰化明胶(GelMA)、聚乙二醇二丙烯酸酯(PEGDA)、胶原、纤维蛋白、脱细胞基质水凝胶,可调节弹性模量匹配骨骼肌发育需求。
• 功能添加:导电聚合物或金纳米线用于电信号传导;温敏或光敏基团赋予4D形变能力;RGD或层粘连蛋白肽段提高细胞黏附。
• 多相墨水:同轴打印实现“外鞘-内芯”结构,外层提供力学支撑,内层包埋肌母细胞与内皮祖细胞,模拟血管化肌束。
3. 细胞排布——再布“房间”
• 共打印:同轴或并列喷头一次性沉积肌母细胞、神经元、内皮细胞与成纤维细胞,实现多细胞精准分区。
• 定向诱导:微通道顶部预置微电极阵列,打印完成后施加脉冲电场,驱动肌母细胞沿电场方向融合形成多核肌管。
• 神经-肌肉接头:在芯片一端打印神经球,另一端打印肌纤维束,微隧道仅允许轴突通过,形成可药物阻断的神经-肌肉接头(NMJ)模型。
4. 动态培养——再通“水电”
• 电刺激:方波脉冲促进肌管成熟并维持收缩表型。
• 机械拉伸:两侧锚定柱连接线性马达,提供拉伸-回缩循环,模拟日常运动负荷。
• 氧梯度:3D打印的氧气可渗透膜将芯片分为常氧区与缺氧区,研究缺血-再灌注损伤。
• 多传感:集成电化学微电极实时监测乳酸、葡萄糖、氧分压;荧光寿命成像(FLIM)追踪烟酰胺腺嘌呤二核苷酸(NADH)动态,评估代谢状态。
三、应用全景扫描
1. 疾病模型:通过不同来源的肌母细胞、神经元与免疫细胞共培养,SMoC已能在体外再现遗传、神经源性、自身免疫及增龄性骨骼肌疾病的典型病理特征。
2. 药物筛选与毒性评价:平台可模拟药物在骨骼肌中的疗效与脱靶毒性,支持先导化合物优化、联合用药策略及早筛淘汰。
3. 遗传与环境互作研究:结合基因编辑、缺氧或微重力刺激,芯片用于解析特定基因、力学或代谢因子对肌纤维表型的调控机制。
4. 多器官耦合:骨骼肌与骨、神经、血管、肝脏等芯片串联,系统性评估肌肉疾病对远端器官的影响及全身药代-药效关系。
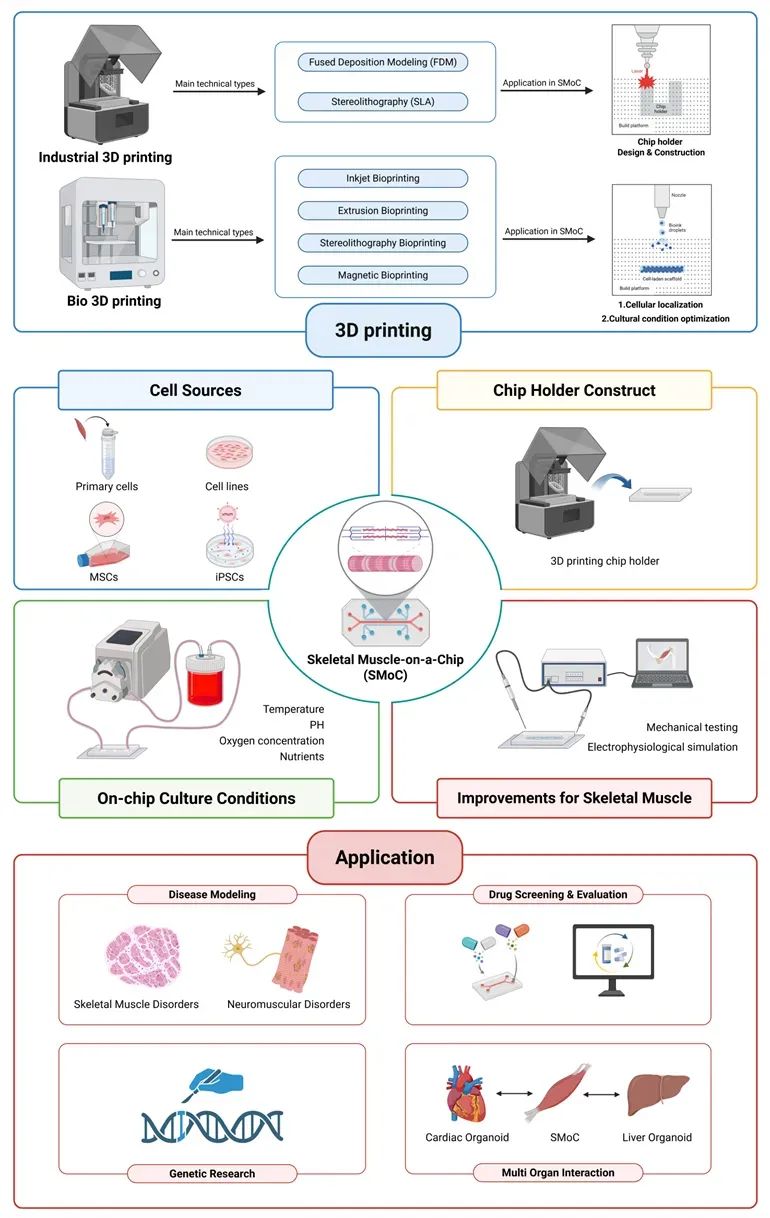
图1. 3D打印技术在器官芯片中的整合与应用
四、技术瓶颈与下一步
1. 打印分辨率:现有光固化生物打印分辨率仍不足以复现肌节级别精细结构。
2. 材料成熟度:高弹性、高导电、可降解且符合GMP标准的墨水体系稀缺;长期培养后的力学稳定性需验证。
3. 功能验证标准:肌力输出、电生理信号、代谢通量尚无行业统一基准,导致实验室间数据难以横向比较。
4. 规模化与成本控制:多喷头阵列打印可提高通量,但喷头堵塞、细胞损伤及无菌操作仍是产业化障碍。
5. 法规与伦理:FDA虽接受器官芯片数据,但对打印过程可追溯性、材料批次一致性、细胞来源合规性提出更高要求。
五、未来展望
1. 4D打印:温度或pH触发的形状记忆水凝胶将在芯片内实现“自卷曲”肌纤维束,模拟肌肉损伤后的自修复过程。
2. AI闭环优化:深度学习算法实时采集收缩视频、代谢曲线与转录组数据,自动调整打印路径、刺激参数与培养基配方。
3. 多器官-多尺度耦合:骨骼肌-骨-关节芯片与循环免疫细胞在线共培养,构建完整“运动单元”;进一步接入肝脏芯片,研究运动代谢产物对全身的影响。
4. 个性化医疗:基于患者MRI数据逆向建模,打印与其解剖学匹配的肌纤维排列角度,实现“一人一芯片”的精准治疗评估。
重庆医科大学的包微副主任医师、刘俊彦硕士、杜承城博士为该文章的共同第一作者;重庆医科大学附属第一医院的黄伟主任、雷一霆主治医师和香港中文大学的李中教授、周良彬博士后为该文章的共同通讯作者。该研究得到了重庆市科卫联合面上项目(2025MSXM019)等资助。
原文链接:
https://www.sciencedirect.com/unsupported_browser


