JCO:伊匹单抗联合尼伏单抗未能改善 MGMT 非甲基化新诊断胶质母细胞瘤患者生存
时间:2025-09-04 12:10:45 热度:37.1℃ 作者:网络
胶质母细胞瘤是成人最常见的原发性脑肿瘤,预后极差。尽管经过最大安全切除、放疗和替莫唑胺化疗联合治疗以及肿瘤治疗场等多模式治疗,患者的总体生存仍然有限。替莫唑胺作为放疗的辅助化疗药物,已被确立为标准治疗,但其疗效主要限于MGMT启动子甲基化的患者,MGMT非甲基化患者通常对替莫唑胺(TMZ)耐药,预后更差。因此,寻找替代或增强治疗效果的新策略尤为迫切。 免疫检查点抑制剂(ICIs)尤其是CTLA-4抑制剂ipilimumab和PD-1抑制剂nivolumab已经在多种实体瘤中显示出显著疗效。早期的一期试验提示这两种药物联合用于新诊断胶质母细胞瘤患者的安全性可接受,且可能存在生存获益,促使开展II/III期随机试验。

本项名为NRG Oncology BN007的随机双盲临床试验,针对MGMT启动子非甲基化(uMGMT)新诊断胶质母细胞瘤患者,评估了双重免疫检查点抑制剂伊匹单抗(ipilimumab,ipi)联合尼伏单抗(nivolumab,nivo)治疗的疗效和安全性。结果显示,该联合免疫治疗方案未能显著改善患者的无进展生存期(PFS),且与标准化疗药物TMZ相比,无整体生存期(OS)优势,提示TMZ仍是该患者群体的标准治疗基石。
研究人员纳入Karnofsky功能评分(KPS)≥70且诊断为MGMT非甲基化的新发胶质母细胞瘤成年患者。患者随机分配至两组,一组接受放疗联合ipi和nivo免疫治疗(无TMZ),另一组接受放疗联合标准TMZ化疗。随机分层因素包括递归分区分析(RPA)类别及是否计划使用肿瘤治疗场。免疫治疗启动时禁止使用皮质类固醇。诊断、MGMT状态和无进展生存均由中心评审确认。 放疗采用总剂量60Gy,分30次照射,常规采用收缩场技术。TMZ按标准剂量放疗同期及放疗后辅助化疗。免疫组ipi剂量为1 mg/kg,每4周1次,最多4剂;nivo剂量为3 mg/kg,每2周1次,ipi完成后改为240 mg固定剂量,治疗至疾病进展。肿瘤治疗场仅允许标准治疗组使用。 随访包括常规体格检查、神经功能评估、实验室检测和脑MRI。疾病进展依据2010年RANO标准,放疗后MRI作为基线。进展率和死亡率通过中心盲审确定。主要终点为II期的无进展生存,III期的总体生存。
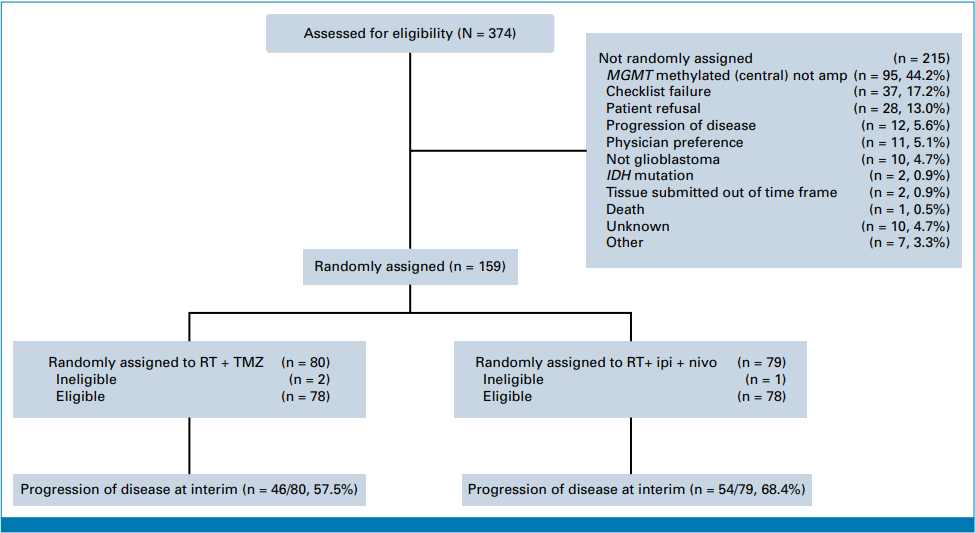
患者入组的 CONSORT 流程图
结果显示,2020年8月试验启动,至2022年4月暂停,共筛查374例患者,随机分配159例(免疫组79例,TMZ组80例)。两组基线特征均衡,患者中位年龄60岁,男性占66%。 数据显示,免疫组中位无进展生存为7.7个月,TMZ组为8.5个月,免疫治疗无显著改善PFS(HR=1.47,70%置信区间1.19-1.83,一侧P=0.96)。总体生存数据尚不成熟,当前中位生存约为13个月,两组无显著差异(HR=0.95,95%置信区间0.61-1.49,P=0.36)。 治疗相关不良事件(AEs)3级及以上在TMZ组和免疫组发生率相似。免疫组报告两例治疗相关死亡(自身免疫性疾病和结肠炎)。 肿瘤治疗场的实际使用率极低,未能对结果构成明显干扰。
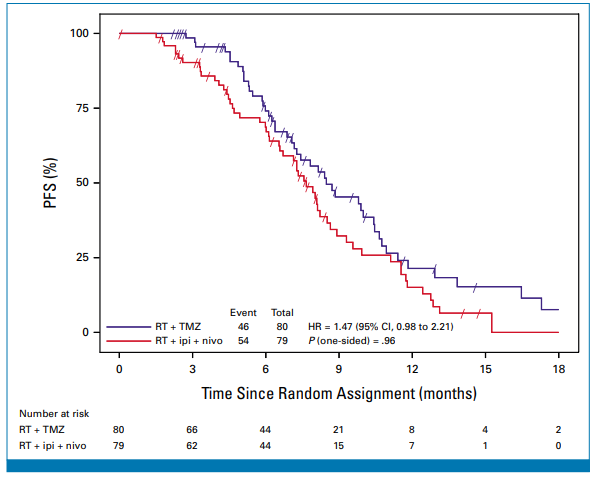
图:按治疗组划分的PFS
总之,ipi联合nivo治疗MGMT非甲基化的新诊断胶质母细胞瘤患者,未能改善无进展生存或总体生存,且安全性无新警示。TMZ仍为该患者群体的标准治疗。未来需探索基于分子标志物的精准免疫治疗策略。试验已永久停止入组,后续分子相关分析及随访仍在进行。当然,该研究也存在一定的局限性。例如不包含MGMT甲基化患者,且排除免疫抑制及使用类固醇患者,限制了结论的普适性。免疫治疗的脑内穿透性和胶质母细胞瘤免疫微环境复杂,可能限制ICI疗效。未来研究应聚焦寻找预测免疫治疗反应的生物标志物,结合多模态治疗优化方案。
原始出处
Andrew B. Lassman et al.Dual Immune Check Point Blockade in MGMT-Unmethylated Newly Diagnosed Glioblastoma: NRG Oncology BN007, a Randomized Phase II/III Clinical Trial. JCO 0, JCO-25-00618.DOI:10.1200/JCO-25-00618
本文相关学术信息由梅斯医学提供,基于自主研发的人工智能学术机器人完成翻译后邀请临床医师进行再次校对。如有内容上的不准确请留言给我们。


