Research 山东大学张梅/戴珅/刘凤鸣合作揭示USP53通过促进RIPK1去泛素化驱动酒精性心肌病进展的新机制
时间:2025-08-29 12:12:48 热度:37.1℃ 作者:网络
酒精性心肌病(ACM)是指由长期过量饮酒引发的扩张型心肌病,酒精诱导的心肌细胞死亡是心室重构和心力衰竭的主要病理机制。据报道,受体相互作用蛋白激酶1 (RIPK1)作为控制细胞死亡途径的关键介质在ACM中发挥重要作用,但酒精诱导心肌细胞RIPK1激活的具体机制尚未见报道。
RIPK1受到多种翻译后修饰(泛素化、去泛素化和磷酸化等)的严密调控。泛素特异性蛋白酶53 (USP53)在心脏组织中高表达,其依赖去泛素酶催化活性可诱导多种癌症细胞死亡,表明其与细胞死亡调控密切相关。然而,USP53在ACM发病和病程进展中的作用机制尚不明确。
2025年8月14日,山东大学齐鲁医院心内科、络病理论创新转化全国重点实验室张梅教授团队和山东大学基础医学院戴珅、刘凤鸣团队合作,在Research上发表了题为“USP53 Drives Ethanol-Induced Myocardial Injury by Promoting K63 Deubiquitination-Dependent RIPK1 Activation at K377”的研究论文,阐明了USP53通过去除RIPK1上赖氨酸(K)377位点的K63泛素链,促进RIPK1依赖性凋亡和程序性坏死,加重ACM发生、发展的作用。

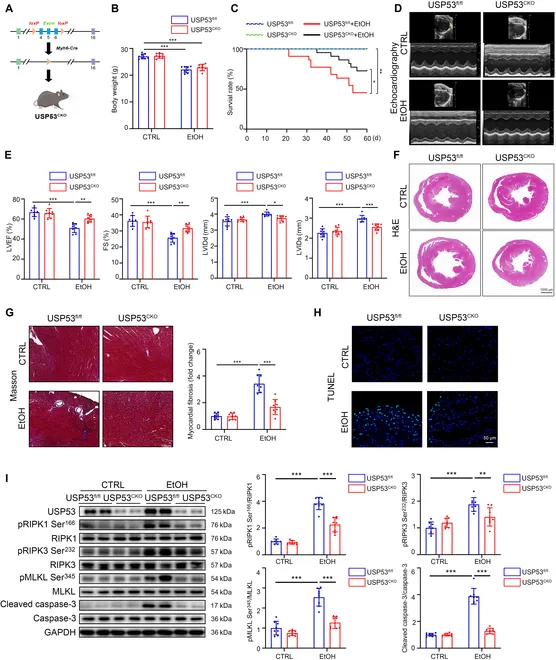
作者首先在体内和体外构建ACM模型。在体内,酒精诱导小鼠心脏出现显著收缩功能障碍,伴随心室腔扩大、纤维化增加。同时,酒精诱导心脏组织和心肌细胞中凋亡标志蛋白cleaved caspase3和程序性坏死标志蛋白pRIPK3、pMLKL显著升高。TUNEL染色和电镜结果进一步显示酒精诱导心肌细胞发生凋亡和程序性坏死。
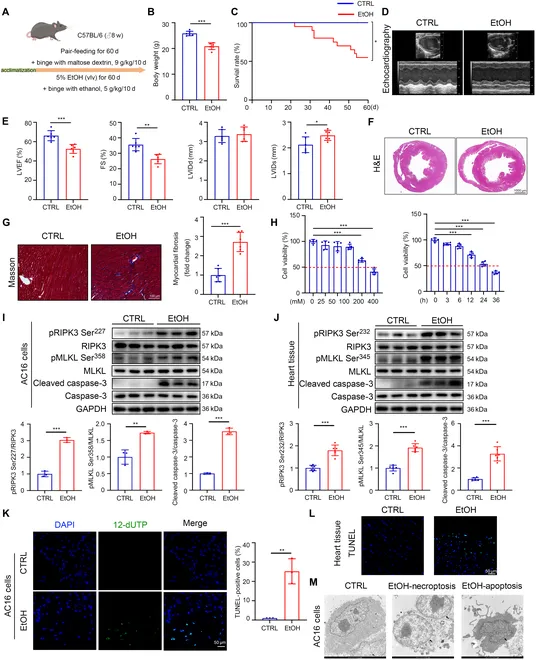
鉴于RIPK1是调控凋亡和程序性坏死的关键上游因子,作者进一步研究发现酒精诱导心脏组织和心肌细胞中RIPK1激酶活化形式—pRIPK1 Ser166显著升高,但RIPK1无显著变化。为了验证RIPK1激酶活化在ACM中的作用,作者在体内和体外分别给予RIPK1激酶抑制剂Necrostatin-1 (Nec-1)处理。在体内,Nec-1显著改善小鼠心脏收缩功能障碍,伴随心室腔变小、纤维化减少。同时,Nec-1能显著抑制心脏组织和心肌细胞中凋亡和程序性坏死以及RIPK1磷酸化。
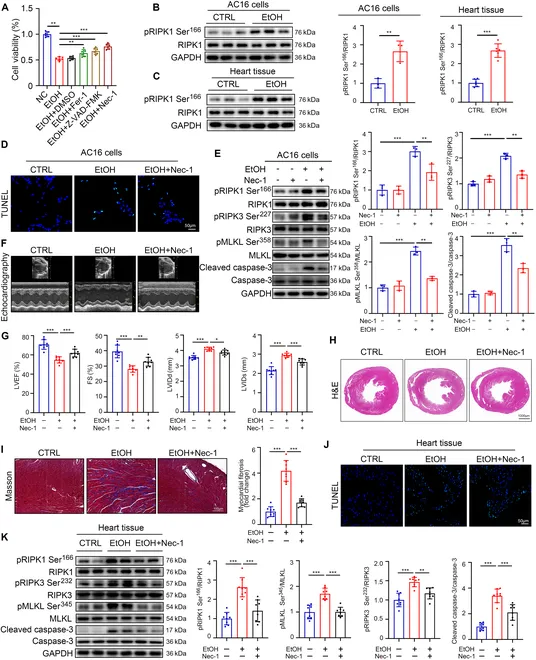
RIPK1激酶活性激活与RIPK1泛素水平密切相关。作者发现,酒精诱导RIPK1泛素水平明显降低。然而,去泛素酶CYLD和E3泛素连接酶cIAP1、cIAP2在酒精刺激下无显著变化。为了探究酒精诱导RIPK1泛素水平降低的具体机制,作者通过Co-IP联合LC-MS/MS分析发现酒精诱导USP53与RIPK1相互结合。同时,进一步研究发现酒精诱导心脏组织和心肌细胞中USP53显著升高,敲低或过表达USP53能够显著抑制或促进酒精诱导的RIPK1依赖性凋亡和程序性坏死。

通过一系列体外实验,作者进一步明确酒精诱导USP53与RIPK1在细胞中相互结合。随后,为确定USP53与RIPK1结合的关键结构域,作者分别构建了4种HA标签的RIPK1截短突变体和2种Flag标签的USP53截短突变体,通过Co-IP实验发现RIPK1的ID结构域和USP53的C端结构域是二者相互结合的关键结构域。
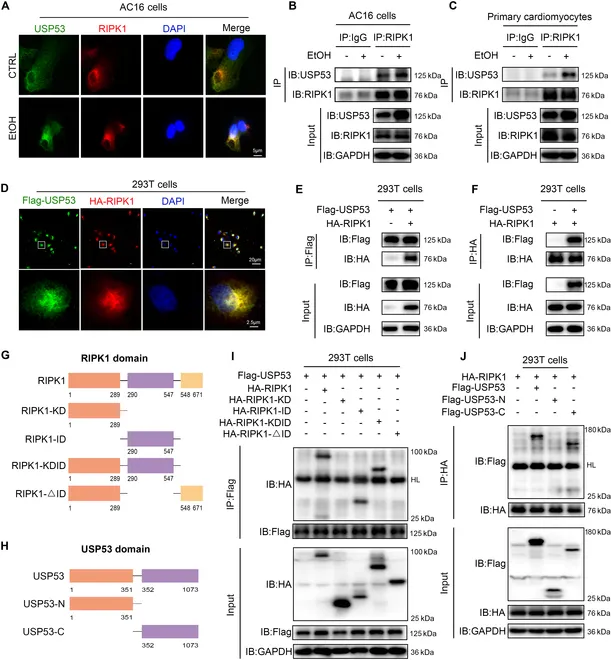
随后,作者进一步研究了USP53调控RIPK1泛素水平的具体机制,发现USP53依赖其去泛素酶催化活性去除RIPK1上K63泛素链。USP53无酶活性突变USP53-C41S不能去除RIPK1上K63泛素链,同时也不能促进酒精诱导的RIPK1依赖性凋亡和程序性坏死。同时,通过突变RIPK1上ID结构域中已知的泛素修饰位点,作者发现USP53调控RIPK1上K377位点泛素水平。

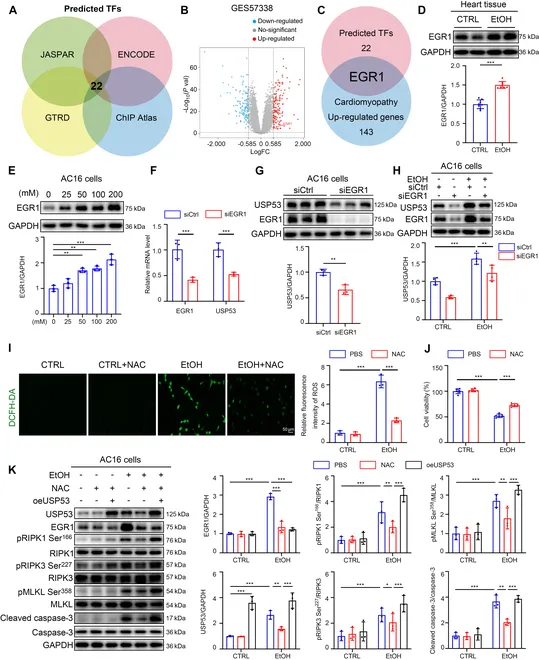
为探究酒精诱导USP53表达升高的分子机制,作者利用JASPAR、ChIP Atlas、GTRD和ENCODE数据库,筛选出22个USP53的潜在转录因子。利用GEO数据库中心肌病相关数据集GSE57338中的差异表达基因和22个转录因子交叉分析,发现EGR1是唯一重叠分子。作者进一步研究发现,酒精诱导心脏组织和心肌细胞中EGR1显著升高,敲低EGR1能够显著抑制USP53表达,而过表达USP53能够逆转敲低EGR1对凋亡和程序性坏死的抑制作用。
鉴于文献表明ROS是诱导RIPK1依赖性凋亡和程序性坏死的关键介质之一,同时ROS能够调控EGR1表达,作者进一步研究发现酒精诱导心脏组织和心肌细胞中ROS水平明显升高。同时,给予ROS抑制剂N-Acetylcysteine (NAC)能显著降低EGR1和USP53的表达,并抑制RIPK1依赖性凋亡和程序性坏死;而过表达USP53能逆转NAC对RIPK1依赖性细胞死亡的抑制作用。
最后,作者通过构建心肌细胞特异性USP53敲除小鼠,发现心肌细胞特异性敲除USP53能够显著改善小鼠心脏收缩功能障碍,伴随心室腔变小、纤维化减少,同时,能显著抑制心脏组织中RIPK1依赖性凋亡和程序性坏死。
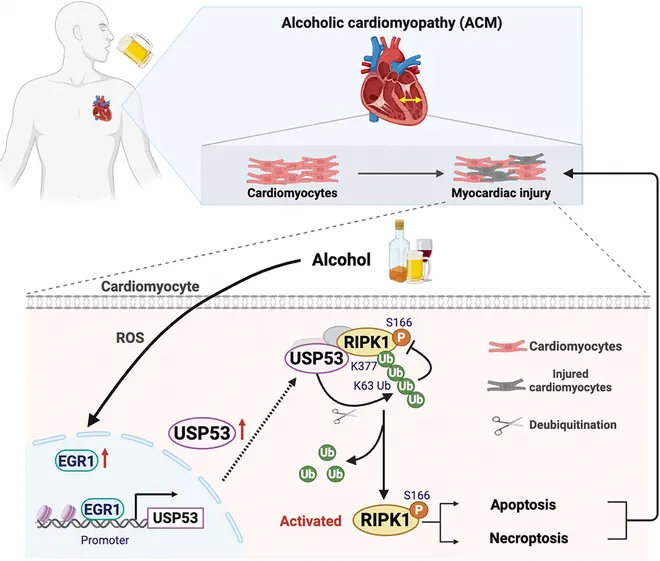
综上所述,该研究发现酒精显著上调心肌细胞USP53表达水平。USP53通过直接结合RIPK1,在K377位点去除K63泛素链,进而激活RIPK1激酶活性,促进凋亡和程序性坏死,加剧ACM。这些发现揭示了USP53在ACM中的关键作用,为ACM治疗提供了新靶点。
山东大学齐鲁医院心内科博士生潘继琛和心内科刘晓琳为该论文的共同第一作者。山东大学齐鲁医院心内科张梅教授和山东大学基础医学院戴珅、刘凤鸣为该论文的共同通讯作者。该研究工作获得国家自然科学基金、山东省自然科学基金、泰山学者计划、中央高校基本科研业务费专项资金以及中国医学科学院非营利性中央研究所基金等项目赞助。
原文链接:
https://spj.science.org/doi/10.34133/research.0823


