【BJH】NDMM中单等位基因缺失和/或主克隆中1p32.3缺失为不良预后
时间:2025-09-16 12:27:11 热度:37.1℃ 作者:网络
1p32.3缺失(del(1p32.3),包含CDKN2C基因)是多发性骨髓瘤(MM)中一个重要的预后标志物,但其在中国临床实践中并未常规检测,临床意义尚不明确。因此苏州大学第一附属医院开展研究,探讨了 1p32.3缺失(del(1p32.3)/CDKN2C) 在中国新诊断多发性骨髓瘤(NDMM)患者中的临床意义及预后影响。近日发表于《British Journal of Haematology》。

研究方法&结果
研究方法
研究纳入345例NDMM患者,所有患者接受VRD(来那度胺+硼替佐米+地塞米松)诱导治疗,其中232例接受自体干细胞移植(ASCT)。结合荧光原位杂交(FISH)和高密度CytoScan芯片技术进行细胞遗传学分析,评估del(1p32.3)的临床特征、治疗反应和预后意义。
研究结果
总人群中,染色体1异常发生率为64.1%,其中1q21获得/扩增占54.8%,1p缺失占25.5%。
40例(11.6%)患者存在del(1p32.3)。该缺失与1q21获得/扩增(85.0% vs 50.8%, p<0.0001)和del(17p)(27.5% vs 12.8%, p=0.0280)显著相关。
del(1p32.3)患者更易伴有髓外病变(EMM)(25% vs 9.8%, p=0.0032)和复杂核型。
与无1p32.3缺失的患者相比,del(1p32.3)患者的无进展生存期(PFS,中位33个月 vs 66个月, p=0.0033)和总生存期(OS, p=0.0403)更差。
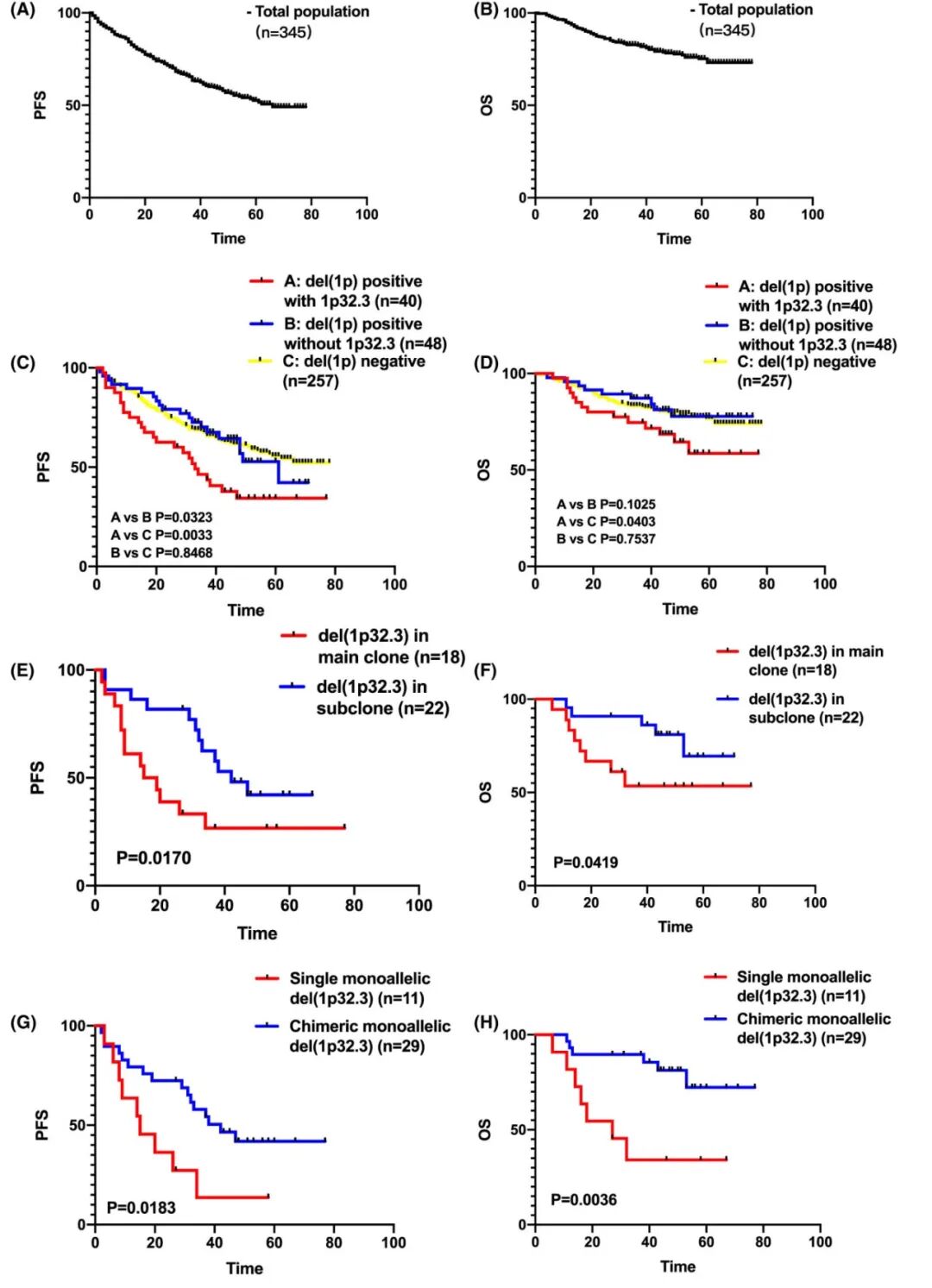
关键发现1: 缺失位于主克隆的患者比位于亚克隆的患者预后更差(中位PFS: 17 vs 42个月, p=0.0170)。
关键发现2: 单等位基因完全缺失(共11例)的患者预后最差(中位PFS: 15个月,中位OS: 27个月),显著差于嵌合型单等位基因缺失(部分细胞缺失)的患者。所有单等位基因缺失均位于主克隆。
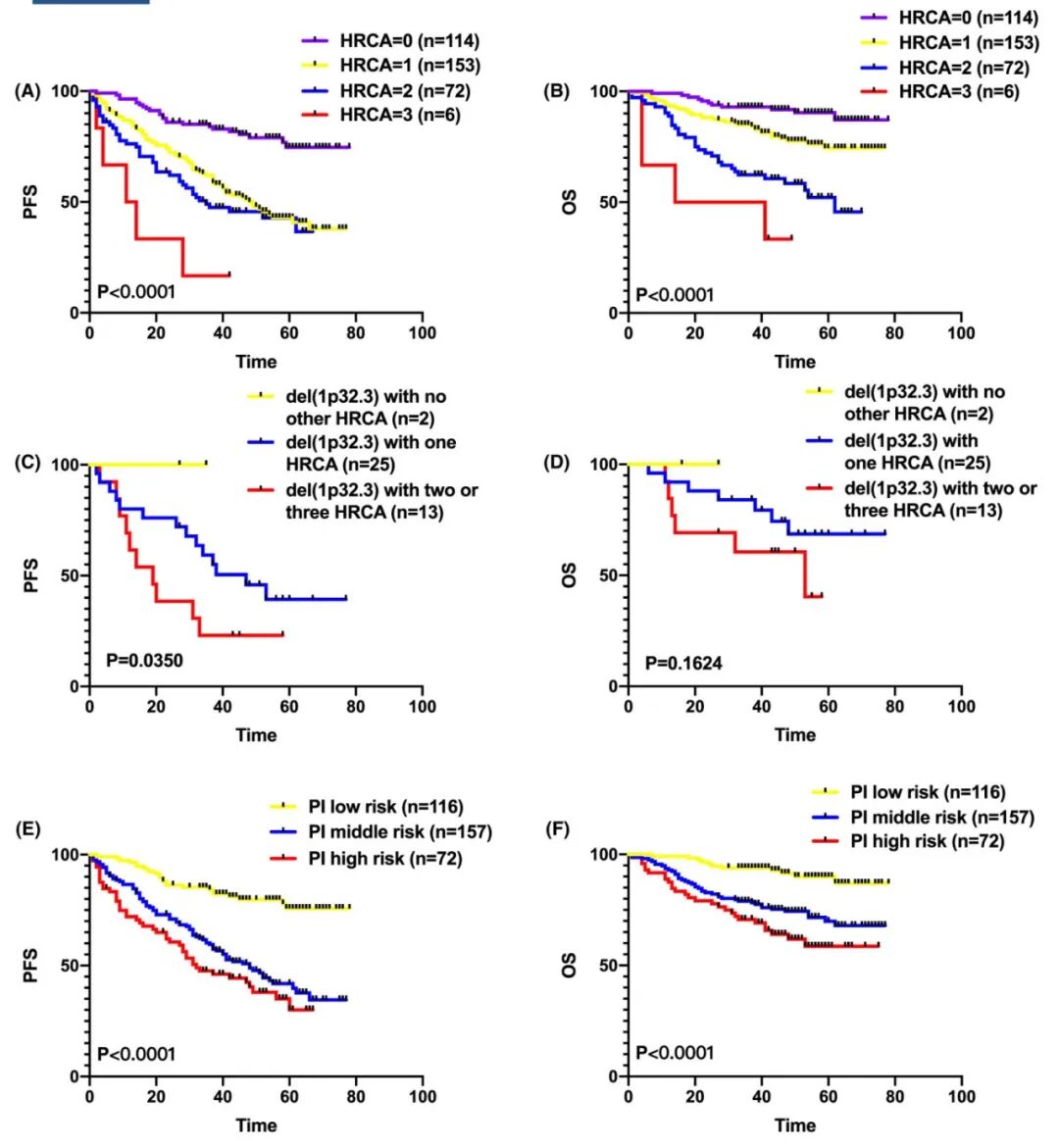
del(1p32.3)与其他高危细胞遗传学异常(HRCA)具有协同恶化预后效应。合并1q21扩增、17p缺失时预后进一步恶化。双/多打击患者中位PFS仅19个月。
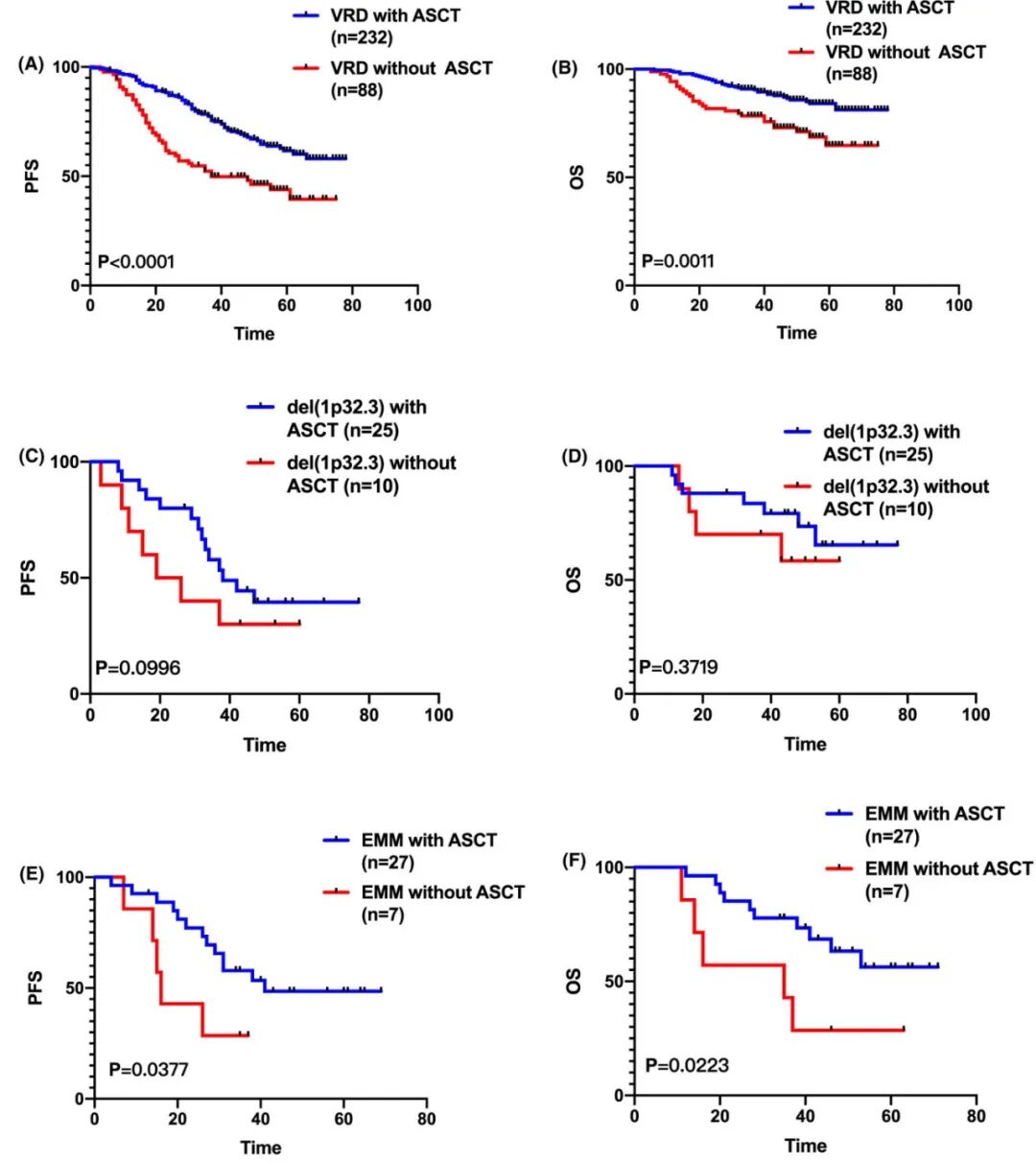
自体干细胞移植(ASCT)虽能改善整体人群预后,但无法完全克服del(1p32.3)带来的不良影响(PFS: p=0.0996; OS: p=0.3719)。ASCT对合并EMM的患者获益显著。
多因素分析显示,del(1p32.3)是PFS的独立不良预后因素(HR=1.597, p=0.047),但对OS影响不独立显著。
总结
1p32.3缺失是新诊断多发性骨髓瘤的独立不良预后因素,尤其是主克隆或单等位缺失时,预后极差,常与1q21获得等协同作用,且不能被ASCT完全逆转。研究者强烈建议在临床实践中将del(1p32.3)纳入常规检测,以进行更精准的风险分层。
参考文献
You H, Yao W, Yan L, Zhai Y, Yan Z, Shang J, et al. Poor prognosis of newly diagnosed multiple myeloma patients with 1p32.3 deletion in single monoallelic deletion and/or in main clone. Br J Haematol. 2025;00:1–12. https://doi. org/10.1111/bjh.70015


