【麻案精析】双侧竖脊肌平面持续阻滞用于多合并症且病态肥胖患者肠切除联合疝修补术后镇痛
时间:2025-09-25 15:47:02 热度:37.1℃ 作者:网络
竖脊肌平面阻滞是一种安全有效的镇痛方法,在其他镇痛方案无效或不适用时可采用,且可作为硬膜外麻醉的潜在替代方案。2025年9月12日,Am J Case Rep刊发来自拉脱维亚里加斯特拉京斯大学的病例报告,详细阐述了对1例剖腹术后患者实施双侧竖脊肌平面持续阻滞的有效过程,既解决了患者因多种合并症带来的临床复杂性问题,也重点应对了术后需重启抗凝治疗这一核心挑战。

病例
患者,男性,64岁,因计划行腹壁前侧大疝修补术入院。该患者此前曾在另一家医院因腹壁前侧疝接受过疝修补术。患者BMI为44.8,身高173cm,体重134kg。合并症包括Ⅱ期肺动脉高压、痛风及慢性阻塞性肺疾病,且病情控制不佳——2019年曾因上述疾病诱发深静脉血栓,此后长期服用利伐沙班(20mg/日)抗凝治疗。
为确保患者与术者均能充分做好术前准备,术前对患者进行腹部CT检查。结果显示胃中部水平存在巨大腹疝,白线处疝颈大小为10×10cm;疝内容物包括大网膜脂肪及回肠肠袢,未见嵌顿征象(图1)。
术前麻醉医师对其进行评估,以确保术前准备充分,并获取了患者对全身麻醉及必要时区域镇痛的知情同意。患者ASA Ⅲ级。评估时发现患者未规律服用处方抗凝药物,因此术前5天开始给予低分子肝素(3500 IU/日)皮下注射。医师已向患者充分告知操作相关风险,患者表示理解并同意。
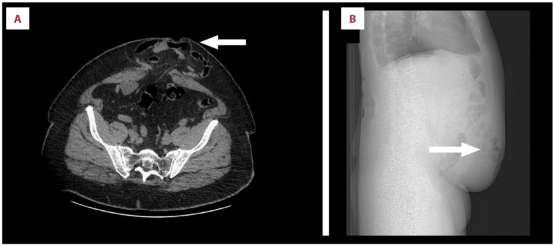
图1 术前CT成像显示腹壁前侧胃中部区域存在巨大腹疝(白色箭头所示)疝囊左右径15cm、前后径6cm、头尾径11cm;疝囊下极略超过脐水平,导致局部皮肤轻微褶皱,上极位于剑突下约13cm处。
患者于手术当日入院,术前口服咪达唑仑7.5mg镇静。全身麻醉诱导用药为:芬太尼0.2mg、丙泊酚200mg、顺式阿曲库铵20mg,随后行气管插管。麻醉维持采用七氟醚(0.9%,氧气-空气混合气体为载气),并根据需要追加芬太尼与顺式阿曲库铵。
手术开始后,先行腹部正中切口,进入腹腔后发现:前次疝修补术植入的补片已与小肠壁粘连生长,形成明显粘连团块;小肠(包括浆膜层)已被补片穿透,导致肠系膜-肠袢分离困难(图2)。此外,一段长1.5m的小肠存在多处粘连、管腔异常及1.5cm长的狭窄性病变。进一步探查腹腔时发现乙状结肠存在缺血改变:一段4cm长的乙状结肠出现黑色斑片状变色,肠系膜浸润,提示缺血坏死性改变(图3)。
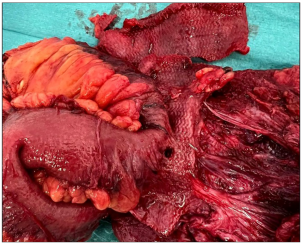
图2切除后的粘连团块,包含前次手术植入的补片;该补片已与小肠(包括浆膜层)粘连生长,导致肠系膜-肠袢无法分离。
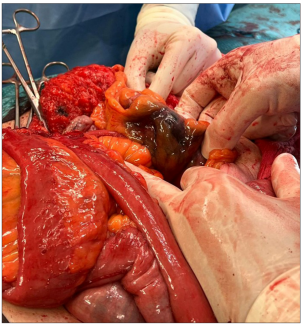
图3乙状结肠肠系膜浸润伴黑色斑片状变色,提示缺血坏死性改变。
鉴于补片与小肠无法安全分离,且乙状结肠存在缺血改变,术者决定行小肠及乙状结肠切除,并随后构建吻合口。肠切除与吻合口重建完成后,再行腹壁前侧疝修补术。最初计划采用腹横肌释放术(TAR),但因术中发现病变范围超出预期、手术时长延长及患者合并症较多,遂调整疝修补策略——采用20×15cm双组分补片,通过腹膜前(直肠后)技术将补片固定于腹壁前侧腱膜,以封闭疝门。
手术总时长为7小时30分钟,麻醉总时长为8小时15分钟。术中患者血流动力学稳定,共使用丙泊酚350mg、芬太尼0.7mg、顺式阿曲库铵50mg。为预防术后疼痛,手术结束前30分钟静脉给予对乙酰氨基酚1g、安乃近1g、右酮洛芬50mg。术后患者顺利拔管,转入ICU。
患者入ICU后,除已使用的镇痛药物外,还给予芬太尼持续静脉输注(浓度0.01mg/ml,速率5ml/h)加强镇痛。
术后次日晨(距手术约10小时),考虑到患者属于血栓高风险人群且有深静脉血栓病史,为预防血栓事件,给予低分子肝素3500IU皮下注射,启动抗凝治疗。同时采用数字疼痛评分量表(NRS)评估患者疼痛程度,结果显示:尽管已给予芬太尼持续输注,患者NRS评分仍达8-9分,且脐周区域疼痛最剧烈。
鉴于镇痛效果不佳,同时结合患者合并症情况及术后需立即启动抗凝治疗的需求,决定实施双侧竖脊肌平面阻滞并置入导管以进行持续镇痛。医师向患者详细解释操作过程后,神志清醒的患者表示理解并签署知情同意书。
该操作在ICU床旁严格无菌条件下进行。患者取左侧卧位,采用曲阵探头超声引导,通过旁矢状位入路将18G Tuohy针于L3-L4节段双侧插入竖脊肌下方,进针方向为尾端-头端。观察到注射液将竖脊肌从横突骨性轮廓抬起并扩散,以此确认针尖位置准确;排除血液反流后,将导管置入至Th11节段(与需镇痛的皮节区域对应)(图4)。
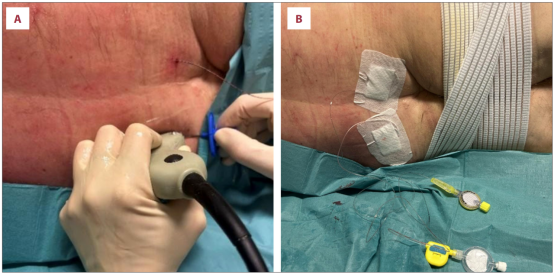
图4(A)L3-L4节段导管置入过程;(B)导管置入完成并确认位置后,准备进行镇痛药物输注。
为进一步确认导管位置,向每侧导管注入造影剂碘海醇(647mg/ml)3ml,随后行X线成像验证。因患者体位及与X线机对齐偏差,成像显示造影剂在图像右侧肋骨区域显影(超出竖脊肌平面阻滞的目标区域)(图5)。
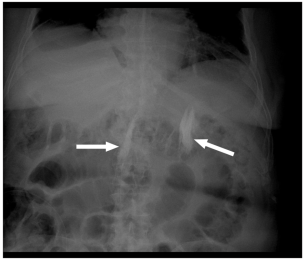
图5白色箭头所示为造影剂显影的T11节段导管位置;因患者体位及与X线机对齐偏差,图像右侧肋骨区域可见造影剂(超出竖脊肌平面阻滞目标区域)。
位置确认后,双侧导管各推注0.125%布比卡因20ml作为负荷剂量,随后以每侧5ml/h的速率启动布比卡因持续输注,并停用芬太尼输注。除布比卡因持续阻滞外,患者还接受对乙酰氨基酚(1g,每8小时1次)及安乃近(1g,每8小时1次)辅助镇痛。在布比卡因输注期间,患者静息状态NRS评分稳定维持在1-2分,无需额外追加芬太尼。
术后第4天拔除阻滞导管,此时患者在继续使用对乙酰氨基酚与安乃近的情况下,疼痛NRS评分仍为1分,随后转入普通外科病房。整个竖脊肌平面持续阻滞过程未出现相关并发症。
转入外科病房3天后,患者病情恶化,复查CT显示乙状结肠旁区域出现血肿,遂决定行手术清除血肿并放置引流。术后患者病情未改善,4天后再次复查CT,发现一处吻合口存在0.8cm缺损,且原血肿区域出现积液。
术者决定再次手术,术中评估发现该吻合口位于后外侧壁,遂保留吻合口并构建结肠造口。两次再手术均未影响初始疝修补效果,未对首次手术结局产生不良影响。术后患者病情逐渐好转,住院33天后顺利出院,出院后未再报告相关并发症。
麻案精析的评述
自2016年Forero等首次在文献中提出竖脊肌平面阻滞(ESPB)以来,这一区域镇痛技术凭借操作简便、安全性高的优势,迅速从胸科手术镇痛领域向多学科手术场景拓展。这例64岁男性在肠切除联合疝修补术这一复杂腹部手术背景下,通过双侧ESPB持续阻滞实现了高效术后镇痛,且成功规避了抗凝治疗与区域阻滞的安全性矛盾。该病例不仅验证了ESPB在特殊人群(多合并症、需抗凝)中的应用可行性,更折射出当前国际上ESPB技术在术后镇痛领域的发展趋势与临床决策逻辑,具有重要的实践参考价值。
传统上,大型腹部手术术后镇痛以硬膜外镇痛为主,但大量研究证实其失败率高达15%-30%,且受限于凝血功能、脊柱解剖异常等禁忌证。该病例中,患者术前合并Ⅱ期肺动脉高压、慢性阻塞性肺疾病及既往深静脉血栓病史,ASA分级Ⅲ级,硬膜外镇痛的风险-获益比显著升高——而ESPB的选择恰好契合了“替代镇痛”的临床需求。
从国际进展来看,ESPB在腹部手术中的应用已形成明确证据链。基于尸体的研究发现,与椎板后阻滞相比,胸段ESPB的局麻药扩散范围更广泛,可覆盖T4-L1皮节,这为腹部手术(尤其是涉及脐周、下腹部区域)的镇痛提供了解剖学基础。该病例进一步延伸了这一证据:通过L3-L4节段入路将导管置于T11水平,精准覆盖疝修补与肠切除的手术区域,最终实现静息NRS评分1-2分的理想镇痛效果,证实ESPB不仅是胸科手术的“常规选择”,更可成为复杂腹部手术的“可靠替代”。
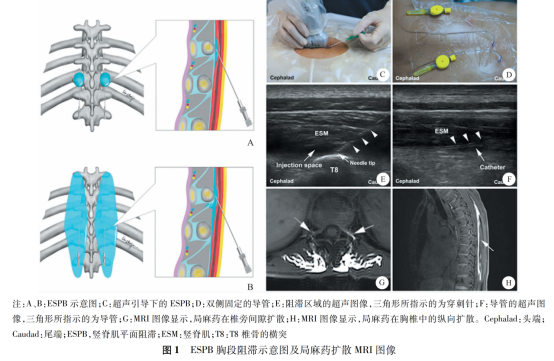
值得注意的是,病例中采用的“持续阻滞”模式具有关键意义。有研究表明,单次ESPB无法满足腹部手术(如腹股沟疝修补术)的长期镇痛需求,而持续ESPB通过局麻药持续输注(该病例采用0.125%布比卡因5ml/h双侧输注),可维持48-72小时的稳定镇痛效果。
围手术期抗凝治疗与区域阻滞的“安全性矛盾”是临床实践中的核心难题。该病例中,患者因既往深静脉血栓病史,术后10小时即启动低分子肝素抗凝治疗,而ESPB的选择成功规避了硬膜外阻滞可能引发的硬膜外血肿风险。
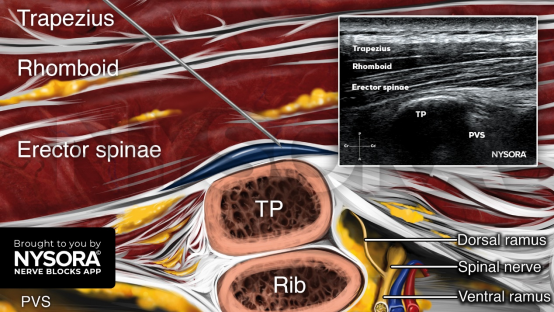
从解剖机制来看,ESPB的局麻药注射部位位于竖脊肌与横突之间的筋膜间隙,远离神经根管、硬膜外腔等富含血管的关键结构。ESPB导管置入位置与神经、心血管系统的“物理距离”,使其严重出血并发症风险显著低于硬膜外阻滞。相关指南将ESPB归类为“低风险区域阻滞技术”,认为其在双联抗血小板治疗(DAPT)、低分子肝素抗凝患者中可安全实施,无需延长停药时间。
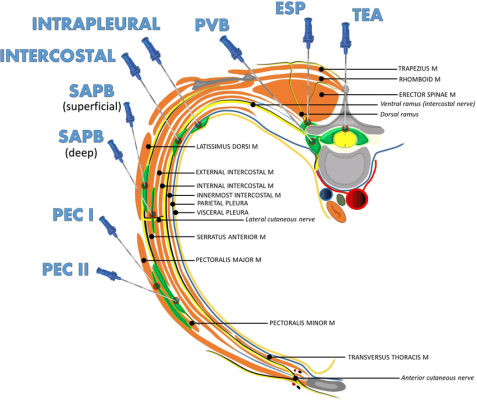
该病例进一步验证了这一安全性:患者在ESPB导管留置期间(术后4天)持续接受抗凝治疗,未出现导管相关出血或血肿,且拔除导管后无残留镇痛失效问题。
该病例的操作细节充分体现了“个体化优化”与“规范化操作”的结合,为临床实践提供了可复制的经验:
其一,超声引导与定位精准性。病例中采用曲阵探头超声引导,通过“旁矢状位入路”与“注射液抬升竖脊肌”的影像学征象确认针尖位置,随后以造影剂(碘海醇)联合X线验证导管位置——这一流程严格遵循国际ESPB操作共识。当前证据表明,超声引导可将ESPB的阻滞成功率提升至90%以上,而造影剂定位则能进一步减少导管异位(如进入胸腔、血管)的风险,尤其对于肥胖患者,超声与影像学联合定位可有效克服脂肪组织对解剖结构显示的干扰。
其二,多模式镇痛的协同作用。病例中在ESPB基础上,联合对乙酰氨基酚(1g q8h)、安乃近(1g q8h)的全身镇痛方案,符合“多模式镇痛”的核心原则,以减少局麻药用量、降低单一药物的毒副作用——该病例中停用芬太尼后未出现镇痛反弹,正是多模式协同作用的直接体现。
其三,并发症的“预防与管理”。病例中术后第4天拔除导管,留置时间控制在临床常规范围内(3-5天),可减少导管相关感染风险;而后续出现的乙状结肠旁血肿、吻合口缺损等并发症,与ESPB无直接关联,且再手术未影响疝修补效果,这提示ESPB不会干扰术后其他并发症的诊断与处理,临床适用性进一步增强。
总之,该病例以“多合并症+复杂腹部手术+抗凝需求”的临床场景为切入点,展现了ESPB在术后镇痛中的核心优势:既是硬膜外镇痛的有效替代,也是抗凝患者的安全选择。从国际视角来看,该病例的操作逻辑与证据应用,与当前ESPB技术的发展趋势高度契合,为临床医师在复杂病例中制定镇痛方案提供了“决策模板”。
原始文献:
Ose G, Evansa I, Krivmanis E, et al. Continuous Erector Spinae Plane Block for Postoperative Analgesia After Intestinal Rep and Hernia Repair Surgery: A Case Report. Am J Case Rep. 2025;26:e949259. doi: 10.12659/AJCR.949259.


