国家纳米科学中心梁兴杰教授,最新Science子刊:纳米囊泡触发胰岛素的特异性释放!
时间:2025-09-28 12:14:44 热度:37.1℃ 作者:网络
糖尿病是一种慢性代谢性疾病,影响全球超过8亿成年人。1型糖尿病(T1D)和晚期2型糖尿病患者需要定期注射外源胰岛素来控制血糖。然而,皮下注射是一种侵入性方法,长期使用会导致患者依从性差。口服胰岛素因其无痛和方便性而受到患者青睐,但面临着胃肠道的恶劣环境、肠上皮的低通透性和肝脏对外来颗粒的快速清除等挑战。
国家纳米科学中心/中国科学院大学梁兴杰、浙江大学王金强、意大利罗马第二大学Massimo Bottini、北京航空航天大学陈军歌等研究人员开发了一种名为MiNVs的纳米囊泡,它能够结合天然IgG,通过FcRn介导的跨细胞运输,避免溶酶体降解途径。MiNVs在到达肝脏后,能够响应肝脏微环境中的高浓度生物硫醇,触发胰岛素的特异性释放。这种纳米囊泡是通过将牛奶来源的外泌体(Miexos)与生物硫醇响应性的胰岛素载脂体(Lipos)通过脂质重排融合而成。相关内容以“Site- specific adaptive nanovesicles for oral insulin delivery”为题发表在《Science Advances》上。

【关键结论】
MiNVs的特性:MiNVs具有良好的稳定性,在模拟胃液(SGF)和模拟肠液(SIF)中表现出比Lipos更好的稳定性。MiNVs在含有GSH的溶液中能够释放胰岛素,而在PBS中则不释放,表明其具有生物硫醇响应性。
体外跨细胞运输:在Caco-2细胞模型中,MiNVs显示出比自由胰岛素和Lipos更高的跨细胞运输效率。MiNVs通过IgG-FcRn相互作用介导的内吞作用进入细胞,并且能够避免进入晚期内体和溶酶体,从而逃避溶酶体降解。
体内分布和吸收:通过在小鼠模型中进行的实验,研究人员发现MiNVs能够在胃肠道中有效分布,并且在肝脏中积累,这表明MiNVs能够通过门静脉将胰岛素有效地递送到肝脏。
血糖控制效果:在STZ诱导的1型糖尿病小鼠模型中,口服MiNVs能够显著降低血糖水平,并且效果持续时间长。此外,MiNVs在1型糖尿病大鼠和迷你猪模型中也显示出良好的血糖控制效果,并且具有较高的口服生物利用度(在大鼠中为20.4%,在迷你猪中为13.3%)。
长期治疗效果:在1型糖尿病大鼠模型中,长期(两周)口服MiNVs治疗能够有效控制血糖,并且在治疗停止后,血糖水平迅速回升,表明MiNVs在治疗期间对血糖的控制是有效的。
【主要内容】
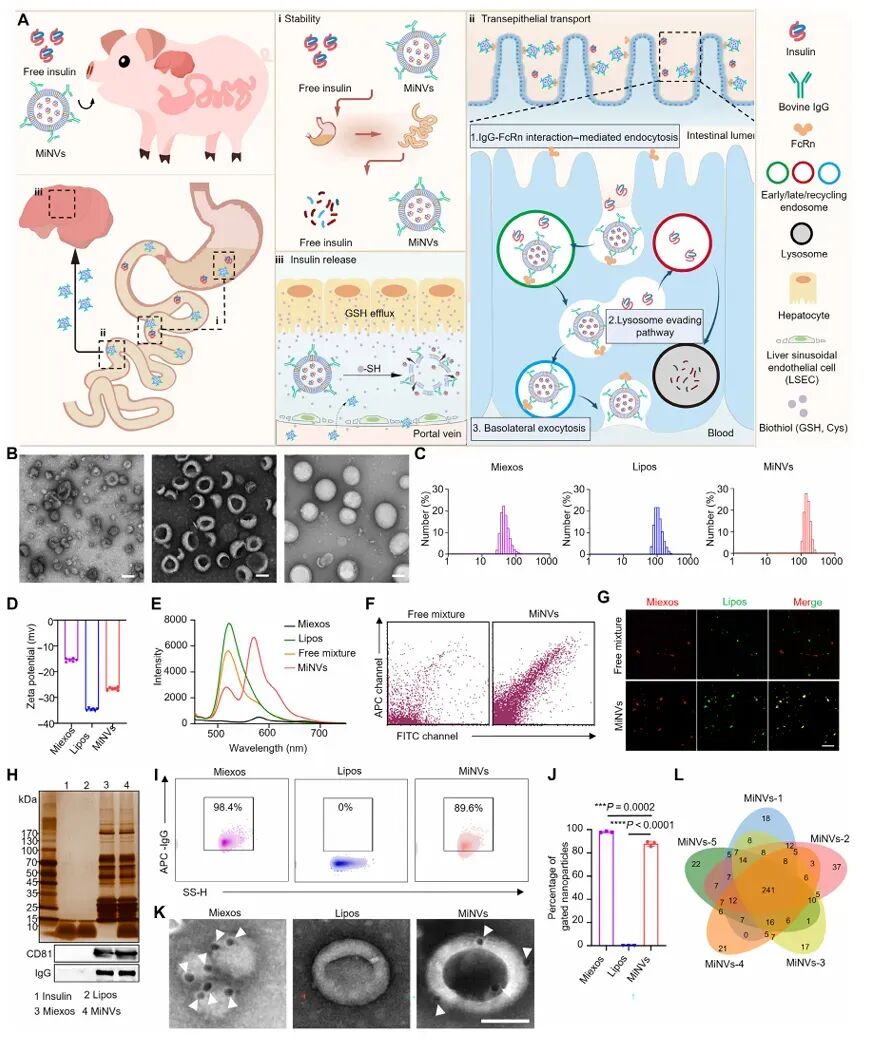
图1:MiNVs的设计原理与特性表征
图中展示了用于口服胰岛素递送的MiNVs的设计原理,包括其通过IgG-FcRn相互作用介导的跨细胞运输以及在肝脏微环境中响应生物硫醇释放胰岛素的过程。同时,对MiNVs的形态、粒径、电位、IgG表达等特性进行了表征,证实了Miexos和Lipos的成功融合以及MiNVs的稳定性和药物包载能力。
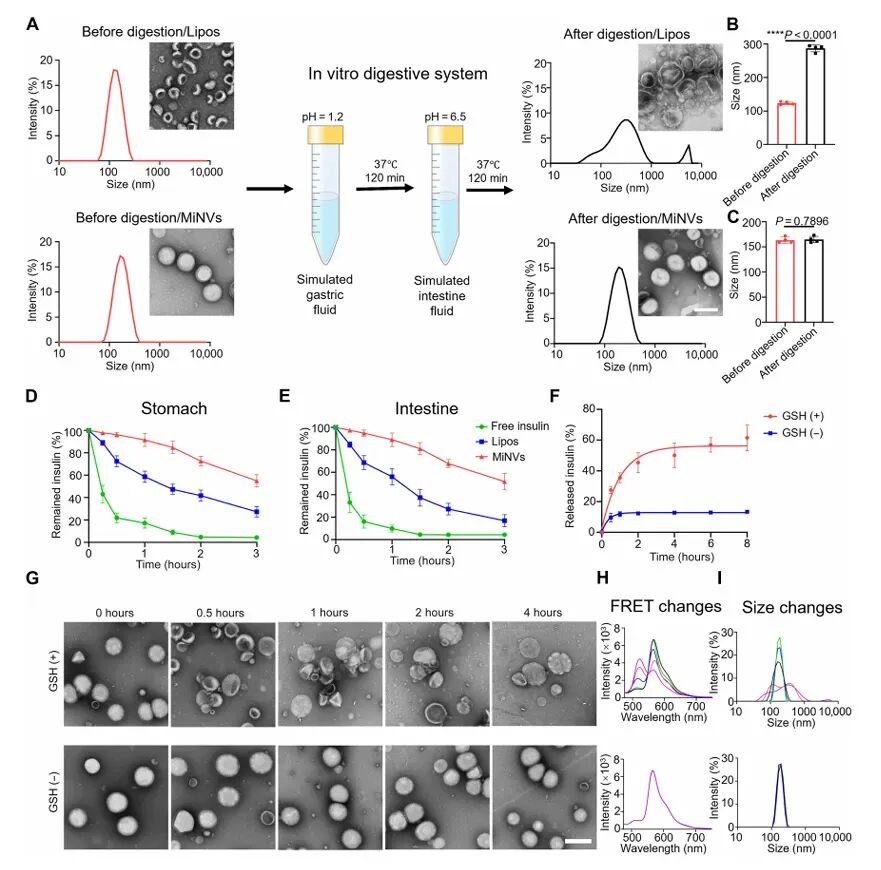
图2:MiNVs的体外稳定性和药物释放特性
进一步研究了MiNVs在模拟胃液(SGF)和模拟肠液(SIF)中的稳定性,结果表明MiNVs在这些条件下具有较好的稳定性,而Lipos则表现出降解和聚集。此外,还探究了MiNVs在GSH溶液和PBS中的胰岛素释放行为,发现MiNVs在GSH溶液中能够响应性地释放胰岛素,而在PBS中则不释放,这验证了其生物硫醇响应性。
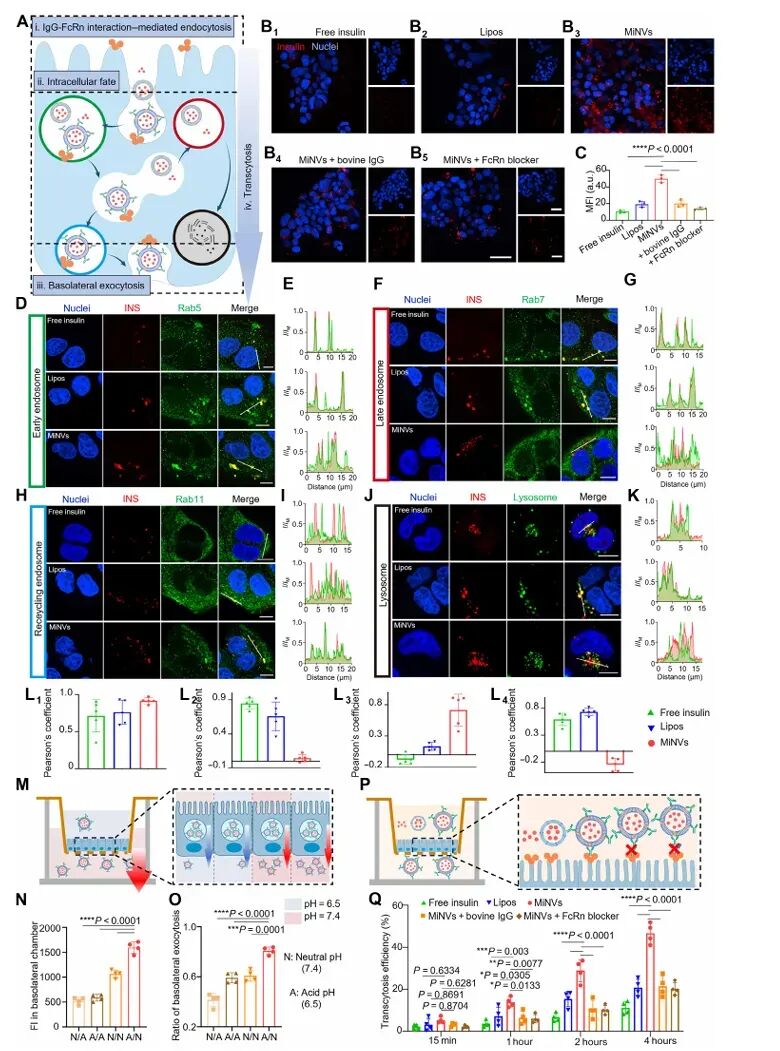
图3:MiNVs的体外跨细胞运输机制
通过Caco-2细胞模型,研究了MiNVs的体外跨细胞运输机制。结果表明,MiNVs能够通过IgG-FcRn相互作用介导的内吞作用进入细胞,并且能够避免进入晚期内体和溶酶体,从而逃避溶酶体降解。此外,还验证了MiNVs在模拟生理pH梯度下具有较高的基底外侧外泌效率,以及其跨细胞运输效率高于自由胰岛素和Lipos。
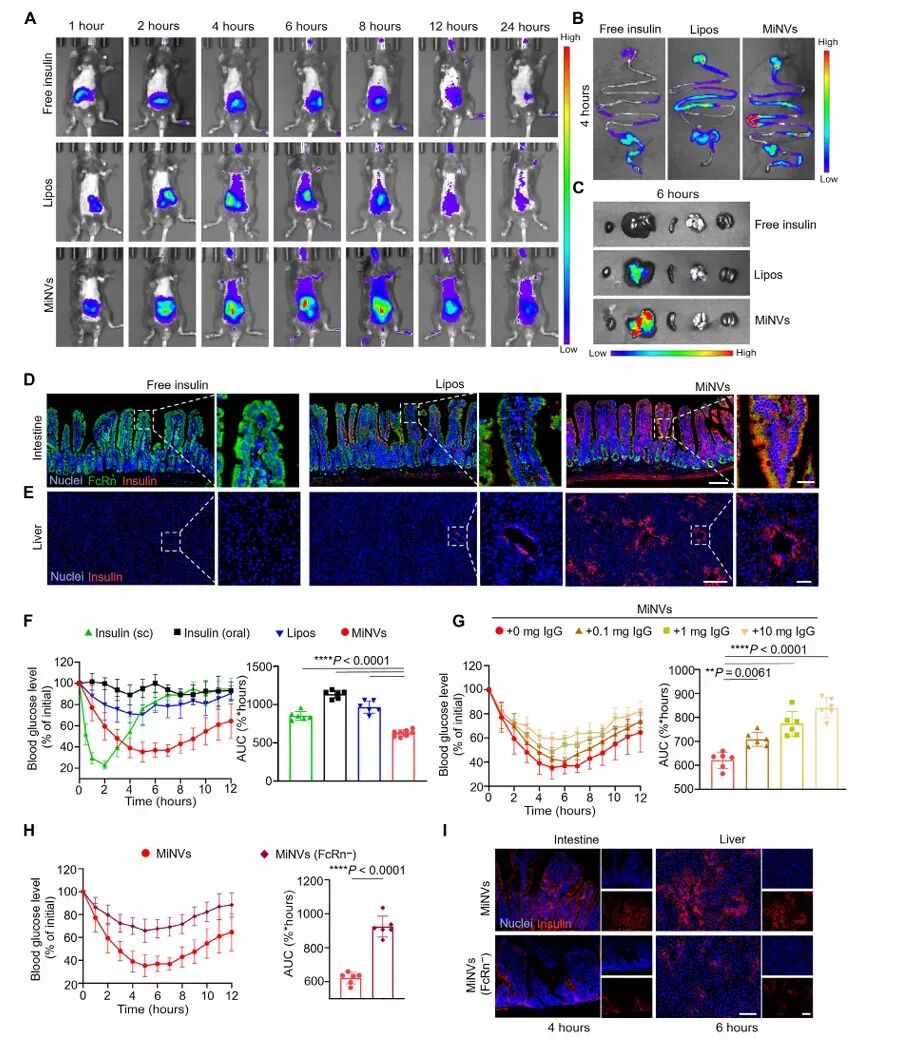
图4:MiNVs的体内分布和IgG-FcRn介导的肠道吸收
通过在小鼠模型中进行的实验,研究了MiNVs的体内分布情况。结果表明,MiNVs在口服后能够在胃肠道中有效分布,并且在肝脏中积累,这表明MiNVs能够通过门静脉将胰岛素有效地递送到肝脏。此外,还通过免疫荧光成像验证了MiNVs在肠道中的IgG-FcRn介导的吸收机制。
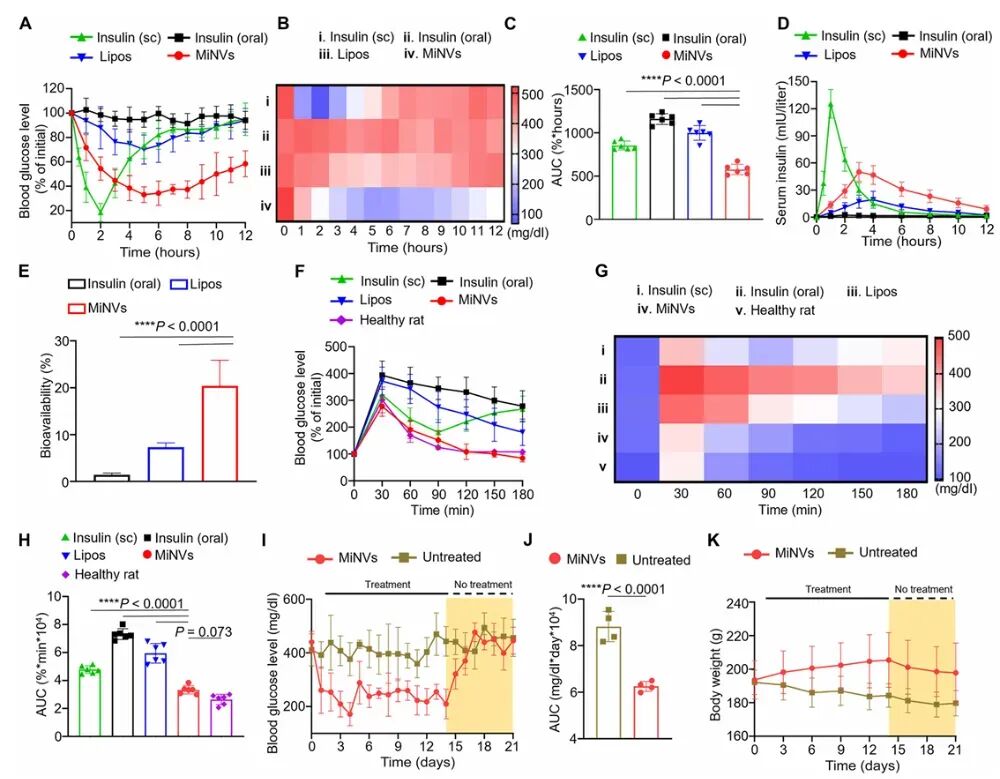
图5:MiNVs在1型糖尿病大鼠模型中的药效学和生物利用度
在STZ诱导的1型糖尿病大鼠模型中,评估了MiNVs的药效学和生物利用度。结果表明,口服MiNVs能够显著降低血糖水平,并且效果持续时间长。此外,还通过药代动力学研究计算了MiNVs的口服生物利用度,并进行了口服葡萄糖耐量测试(OGTT)以评估MiNVs对血糖控制的长期效果。
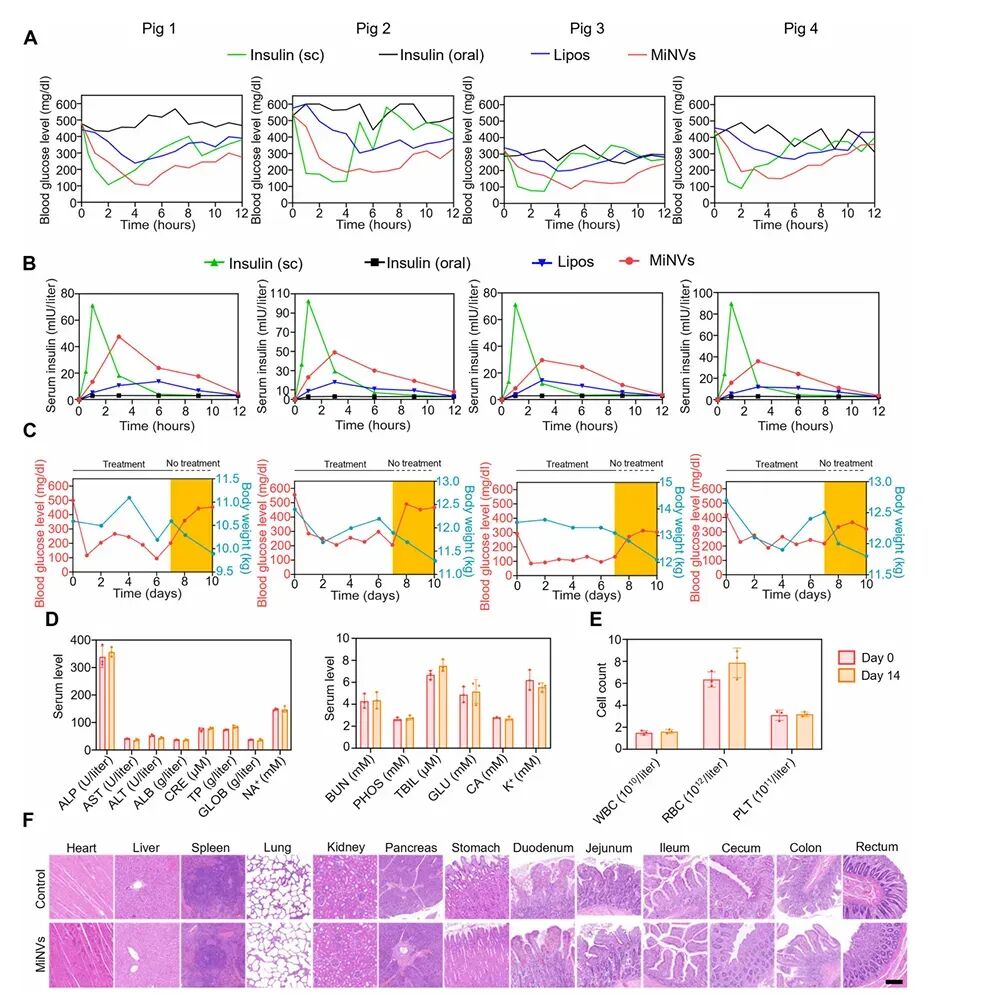
图6:MiNVs在1型糖尿病迷你猪模型中的疗效评估和长期安全性
在STZ诱导的1型糖尿病迷你猪模型中,进一步验证了MiNVs的疗效,并评估了其长期安全性。结果表明,口服MiNVs能够有效降低血糖水平,并且在1周的治疗期间保持稳定的血糖控制。此外,还对健康迷你猪进行了14天的连续口服MiNVs实验,通过血液生化分析和组织学检查,证实了MiNVs具有良好的生物安全性。
【全文总结】
本文介绍了一种新型的口服胰岛素递送系统——牛奶来源的纳米囊泡(MiNVs),它通过结合天然IgG实现FcRn介导的跨细胞运输,避免溶酶体降解,并在肝脏微环境中响应生物硫醇释放胰岛素。在1型糖尿病小鼠、大鼠和迷你猪模型中,MiNVs展现出良好的血糖控制效果和较高的口服生物利用度,同时具有优异的生物安全性,为口服胰岛素治疗提供了新的策略。
原文链接:
https://www.science.org/doi/10.1126/sciadv.ady6386


